運営会社:株式会社つばめLaboについて
株式会社つばめLaboは「世界の医療をボーダーレスにし、あらゆる人に届ける」をミッションとし、インターネットを活用した医薬品の輸出入事業、医療・医薬品の情報提供サービス事業を展開しています。現在、大学病院や研究施設から地域のクリニックまで、400以上の医療機関と取引をしています。

新型コロナウイルス 抗体検査キット
(Biolidics社製)
3営業日以内に出荷いたします。
<送料について>
1箱〜4箱のご注文の場合・・・送料800円(税抜)
5箱以上のご注文の場合・・・送料無料
<ご注文例>
例)1箱のご注文の場合・・・
商品代金:1箱×¥8,000(税抜)=¥8,000
送料:¥800
消費税: ¥8,800×10%= ¥880
合計金額: ¥8,800+ ¥ 800= ¥9,680
<お支払いについて>
・ご注文確定後、請求書を発行致します。
・納品後10日以内にお支払い下さい。
・お支払い方法: 指定指定銀行口座へお振込
本ページの主なコンテンツ
商品情報
| 商品名 | 2019-Novel Coronavirus (2019-nCoV) IgG/IgM Detection Kit (Colloidal Gold) |
|---|---|
| 内容量 | 1箱(10テスト・スポイト10本・緩衝液1個・説明書1枚) * 緩衝液の付属数量と期限については使用説明書をご覧ください |
| 価格 | 1箱=¥800(税抜)×10テスト =¥8,000(税抜) |
| 使用期限 | 2021年4月26日 |
| 製造元 | Biolidics Ltd.(シンガポール) Biolidics社について |
2019-nCoV IgG/IgM抗体検査キット/Biolidics
(新型コロナウィルス抗体検査キット)
- ✓高い感度、特異度、正確度
- ✓血清/血漿/全血に対応 *1
- ✓新型コロナウイルスの2種類の抗体 IgG/IgM を同時に検出


Submission *3 No: PEUA200200

HSA 600:36/01


European CE Marking (DE/CA70/40838-154686)
1 指先を穿刺する採血方法は推奨しておりません。全血、血清、血漿について検証済みです。
2 本製品を用いて全血と血清検体を検査し、結果を臨床診断と比較しました。
3 Biolidics社は、自社の2019-nCoV抗体検査キットの有効性を立証し、米国FDAに通知しました。 この検査キットは、米国FDA指針書※に基づいて流通することになります。 ※「公衆衛生上の緊急事態(2020年3月16日発令)の2019新型コロナウイルス用の診断テストに関するFDAポリシー」(セクションIV.D.に概説) EUA(緊急使用許可)要求を提出済み(提出番号:PEUA200200)。
ダウンロード用ドキュメント
使用説明書比較表
| BIOLIDICS | 商品 A | 商品 B | 商品 C | 商品 D | 商品 E | |
|---|---|---|---|---|---|---|
| 結果までの判定時間 | 10分 | 10分 | 10分 | 10分 | 10分 | 10分 |
| 検体のタイプ | 血清/血漿/全血 | 血清/血漿/全血 | 血清/血漿/全血 | 血清/血漿/全血 | 血清/血漿/全血 | 血清/血漿/全血 |
| 感度(Sensitivity) | 91.54% | 90.2% | 87.3% | 90% | 86.43% | 97.9% |
| 特異度(Specificity) | 97.02% | 99.2% | 100% | 90% | 99.57% | 91.77% |
| 正確度(Conformity) | 95.09% | 95.2% | - | - | 91.61% | - |
| 認証 | CEマーキング/ FDA-EUA提出/ Health Science Authority(SG)/フィリピンFDA | NMPA/CEマーキング | NMPA/CEマーキング | CEマーキング/ FDA-EUA提出 | NMPA/CEマーキング | FDA-EUAに提出 |
Biolidics社の臨床試験データ
| 診断 | 合計 | |||
| 陽性 | 陰性 | |||
| 検査結果 | 陽性 | 184 | 11 | 195 |
| 陰性 | 17 | 358 | 375 | |
| 合計 | 201 | 369 | 570 | |
検査手順等の説明
| 検体のタイプ | 血清 | 血漿 | 全血 |
|---|---|---|---|
| 採血管 | 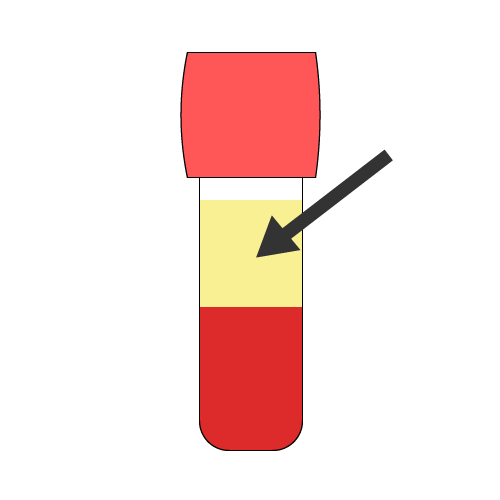 プレーン管(5 mL)ゲルの有無は関係なし | 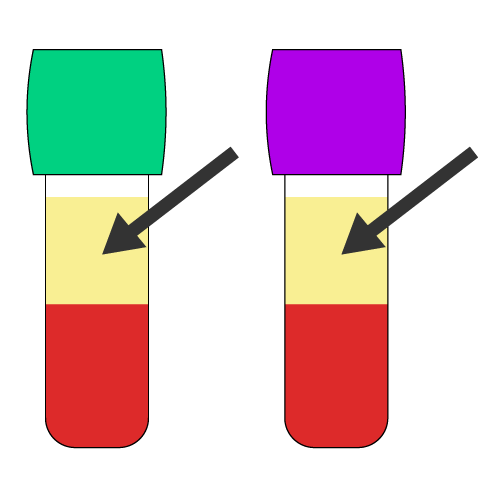 ヘパリンまたはEDTA抗凝固剤入り採血管(3 mL) |  EDTA抗凝固剤入り採血管(3mL) |
| 保存条件 | 血清/血漿は
| 全血は直ちに検査する必要があります。 | |
| その他の重要な注意事項 |
| ||
溶血または高脂血症血液検体は、2019-nCoV IgG/IgM抗体検査キットを用いて検査しないで下さい。
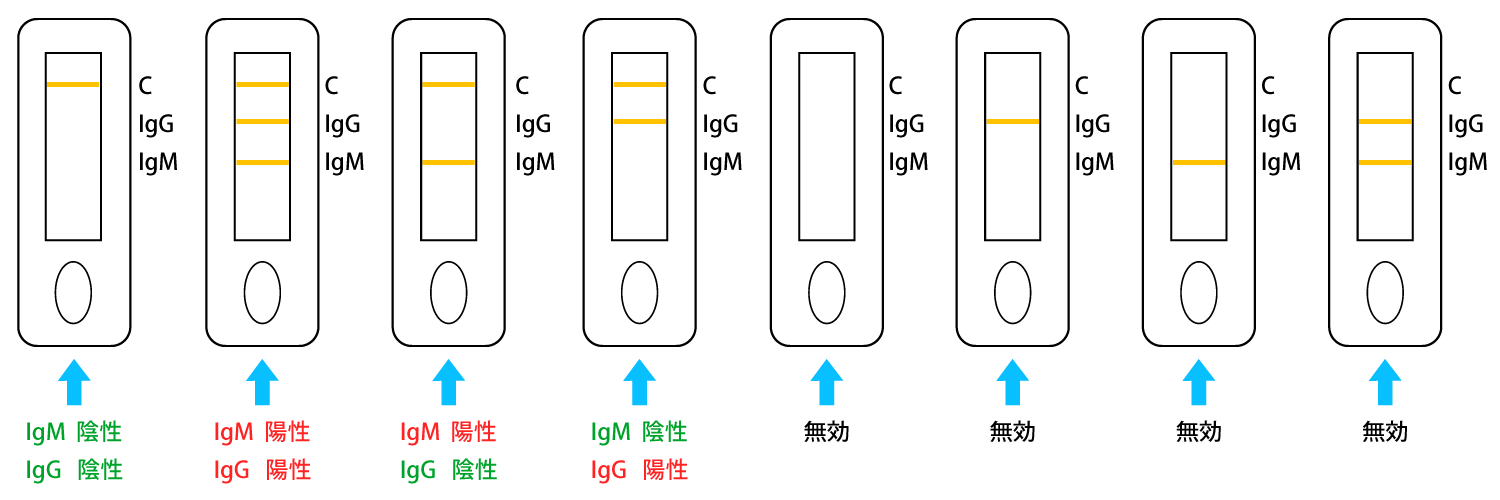
| 結果* | 解釈** |
|---|---|
| IgM 陽性,IgG 陽性 | 新型コロナウイルス(SARS-CoV-2)に最近感染した疑いがある |
| IgM 陽性,IgG 陰性 | 新型コロナウイルス(SARS-CoV-2)に最近感染した疑いがある |
| IgM 陰性,IgG 陽性 | 過去の感染が疑われる |
| IgM 陰性,IgG 陰性 | 新型コロナウイルス(SARS-CoV-2)に対するIgG/IgM抗体が検出されない、または検出限界を下回る抗体レベル |
* Cにラインが表示された場合に限り、結果を評価する必要があります。もし存在しない場合、検査結果を評価せず、破棄する必要があります。検体の再検査が必要になります。
** 本検査は、新型コロナウイルス(SARS-CoV-2)の抗体保持者の特定をサポートすることを目的としています。IgG/IgMの陽性結果は、直近または過去の感染を示しています。本検査は新型コロナウイルス(SARS-CoV-2)の急性感染診断での使用は対象外とし、診断には直接検査の実施が必要です。
よくある質問
- 検査のタイプにはどのようなものがありますか?また、違いは何ですか?
新型コロナウイルス(SARS-CoV-2)を検出する検査には、主に分子検査と血清学的検査の2種類があります。分子検査では、ウイルスの遺伝物質であるRNAを検出します。血清学的検査では、感染に応答した免疫系によって産生される抗体と呼ばれるタンパク質を検出します。 - 新型コロナウイルス(SARS-CoV-2)に対する抗体はいつ現れますか?
感染すると、人体は異なる時点でIgMとIgGを産生します。IgM抗体は通常、感染の初期から中期に産生されるが、IgG抗体は感染の中期から後期に存在し、回復後も存在し続けます。詳しくはこちらをご確認ください。 - 検査は誰が行う必要がありますか?
検査を実施できるのは、医療従事者か研究者に限ります。 - 自宅で個人的に使用するために検査キットを購入できますか?
いいえ。販売は医療機関または研究機関に限ります。また、試験研究用としての使用に限定されます。 - 緩衝液の付属数量と期限について教えてください
緩衝液は1箱に1本付属されています。緩衝液の使用期限は開封から1ヶ月になります。(製品自体の使用期限は製造から6ヶ月)。 詳細につきましては使用説明書をご確認下さい。 - 感度、特異度、正確度の違いは何ですか?
詳しくはこちらをご確認ください。 - EUA(緊急使用許可)とはどういう意味ですか?
2020年2月4日、米国保健福祉省(HHS)の書記官は公衆衛生上の緊急事態があると判断し、FDAのクリアランスを受けることなく、新型コロナウイルスの検出および診断のための体外診断に対して緊急使用許可(Emergency Use Authorization)を発行しました。EUAの承認を受けた検査はFDAによるレビューを受けていますが、その使用はEUAの期間中に限り承認され、FDAの認可または承認を受けていません。
使用目的と注意事項
- 2019-nCoV IgG/IgM抗体検査キット(金コロイド)は、医療従事者や研究者が採取したヒト血清、血漿、全血中に含まれる新型コロナウイルス(SARS-CoV-2)に対するIgG/IgM抗体の定性的検査を目的とします。また、本製品は、体外診断用医薬品ではなく、新型コロナウイルス(SARS-CoV-2)の抗体の有無を見るための試験研究用としての使用に限定されます。
- 本検査で得られた結果を、新型コロナウイルス(SARS-CoV-2)感染の診断、除外、または感染状態の唯一の根拠として使用しないで下さい。結果は臨床症状と合わせて解釈し、補足検査(RT-PCRなど)で確認する必要があります。
- 本キットは、指先の穿刺検査、自宅での検査、または献血のスクリーニングを目的としたものではありません。
- 本製品は日本国内の薬事承認を受けておりませんので、体外診断用医薬品ではございません。
- 本製品の使用は、試験研究用に限定して販売しております。
- 本製品は現在 FDA-EUA の申請中です。
- 本製品の使用による発生した損害及び損失について、弊社は責任を負いません。
- 特に新型コロナウイルス(SARS-CoV-2)に接触したことがある人では、結果が陰性でも新型コロナウイルス(SARS-CoV-2)感染が否定されるわけではありません。
- 本製品は、新型コロナウイルス(SARS-CoV-2)に対するIgMおよびIgG抗体の存在に対してのみ認められており、他のウイルスや病原体に対しては認められていません。
感度とは?特異度とは?
昨今、抗体検査やPCR検査の感度や特異度について議論がなされています。
疾患のある人は100%陽性になり、疾患のない人は100%陰性となるような検査が理想ですが、臨床検査においてこのような検査はほとんどなく、疾患のある人も陰性となったり、疾患のない人でも陽性になったりすることがあるのが現状です。
ここでは、検査精度を規定する指標となる感度や特異度について分かりやすく説明していきます。
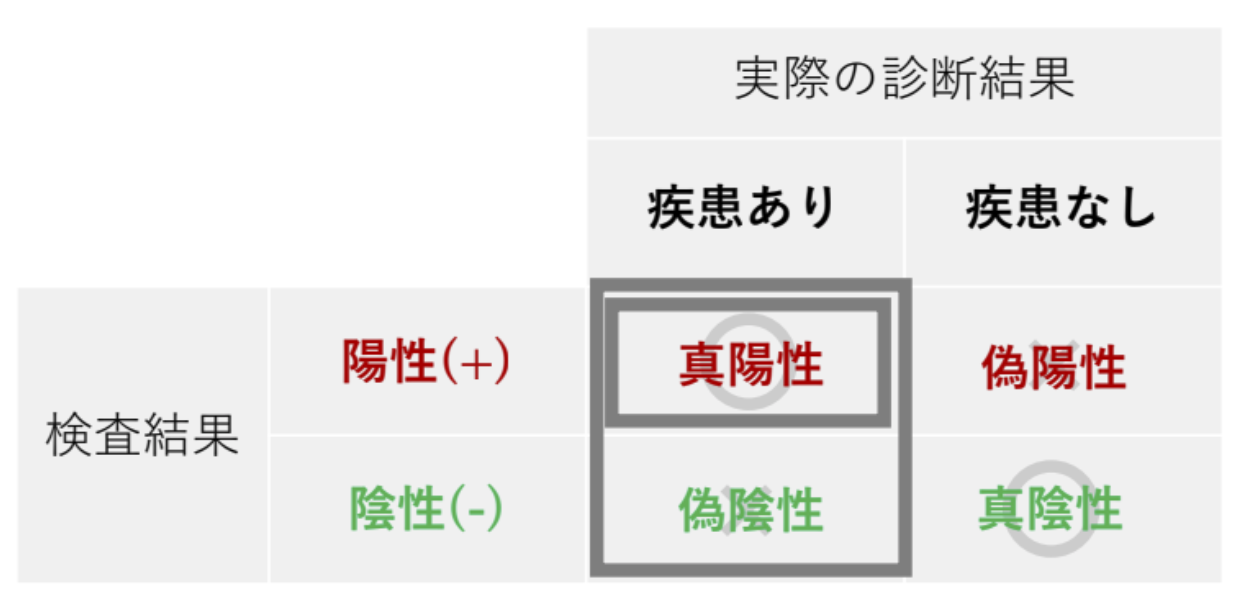
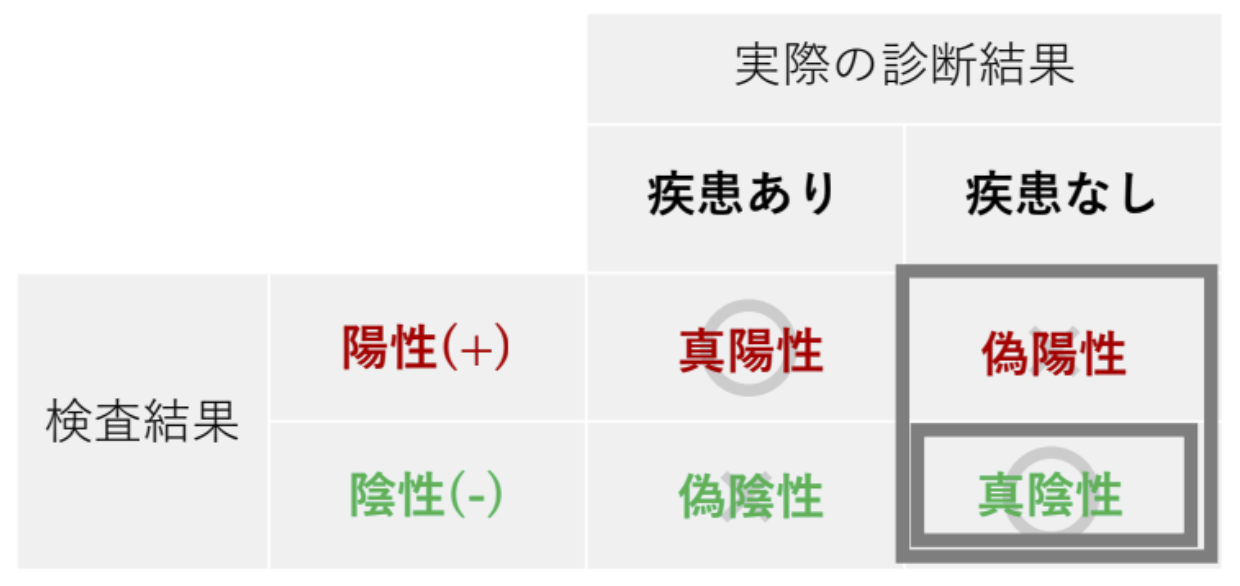
例えば、検査結果の判定と実際の疾患の有無を正誤表にしたのが以下のクロス表になります。

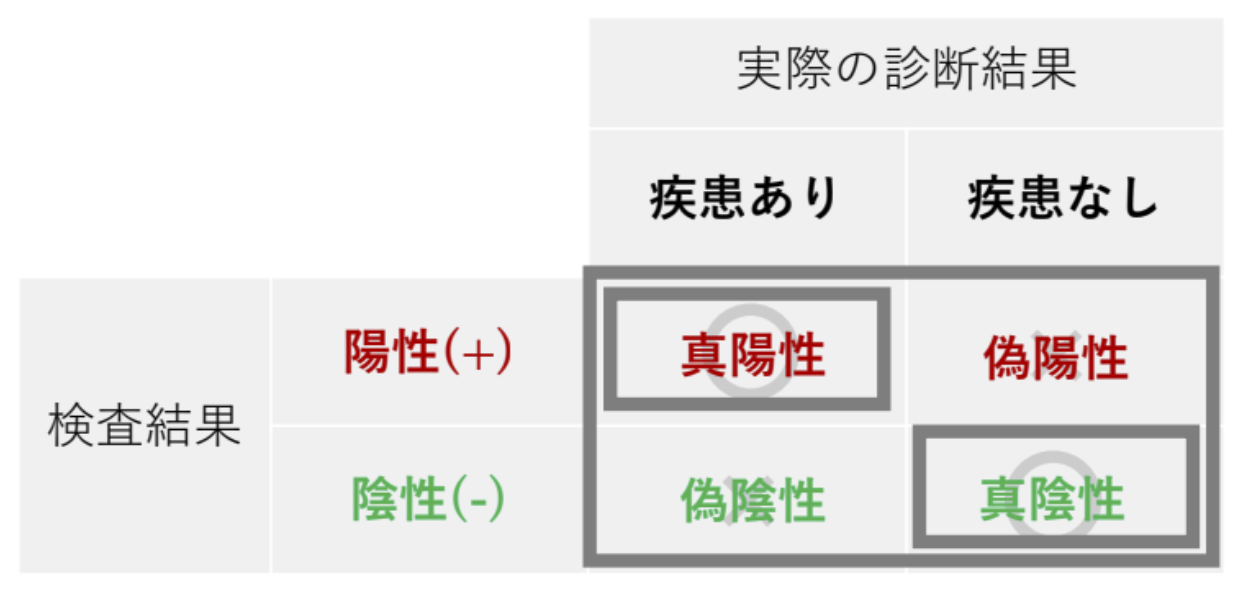
検査結果と疾患の有無が一致する左上と右下が「正答」になり、左下と右上が「誤答」になります。 そして、「正答」に「真」、「誤答」に「偽」という言葉を用いたのが以下のクロス表です。

まとめると以下のような表現になります。
・検査結果が「陽性」で「正答」(疾患あり)のものを「真陽性」
・検査結果が「陽性」で「誤答」(疾患なし)のものを「偽陽性」
・検査結果が「陰性」で「正答」(疾患あり)ものを「真陰性」
・検査結果が「陰性」で「誤答」(疾患なし)のものを「偽陰性」
そこで、この検査結果に対して、複数の指標を使って精度を評価したものが「感度」や「特異度」「正確度」と言われるものになります。
感度(Sensitivity)
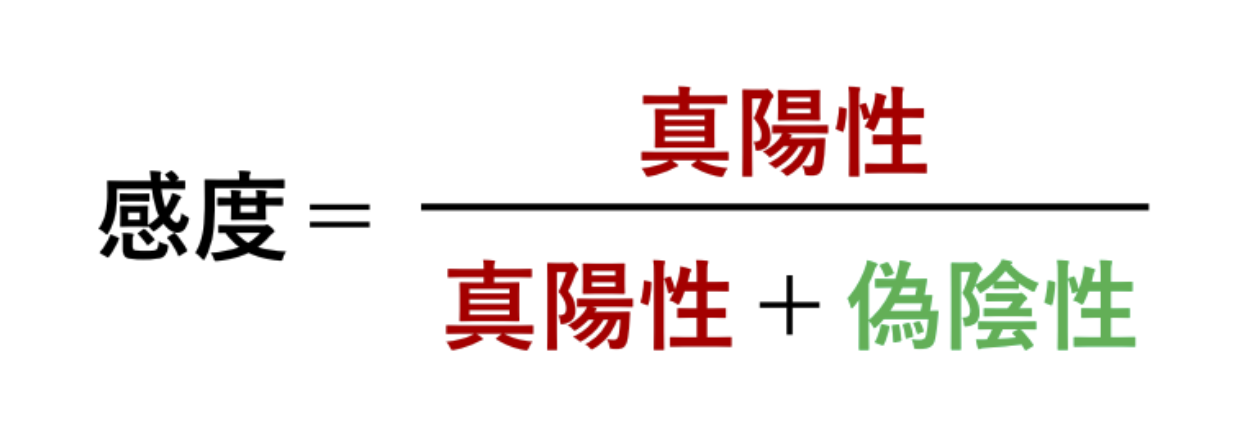
感度とは疾患のある人を正しく疾患があると判定する確率になります。
逆に言えば、疾患がある人を問題なしと判定してしまうこと、つまり「見逃し」がないかをみる指標になります。感度の計算は真陽性の数を、疾患ありの総数 (真陽性 + 偽陰性) で割ります。感度が高ければ高いほど疾患のある人を見逃さないことになりますので、感度は検査の精度を規定する重要な指標と言えます。
特異度(Specificity)
特異度とは疾患のない人を正しく疾患がないと判定する確率になります。
逆に言えば、疾患のない人を疾患があると無意味に疑うような誤診がないかをみる指標になります。特異度の計算は真陰性の数を、疾患なしの総数 (偽陽性 + 真陰性) で割ります。特異度が高ければ高いほど、疾患のない人までむやみに疑う確率が低くなると言えます。

正確度(Conformity)
正確度とは全体の正答率になります。正確度の計算は正答のもの (真陽性 + 真陰性) の数を、全体の数で割ります。

<参考文献>
Gordon Guyatt 他編『臨床のためのEBM入門―決定版JAMAユーザーズガイド』医学書院 ,2003年
抗体検査とは?PCR、抗原検査との違いは?
| 抗体検査 (感染による血液中の抗体を検知) | PCR検査 (ウィルスを検知) | 抗原検査 (ウィルスを検知) | |
|---|---|---|---|
| 目的 | 過去の感染の有無(抗体の有無)を判定 | 現在感染しているかを判定 | 現在感染しているかを判定 |
| 検体 | 血液 | 鼻咽頭ぬぐい液 | 鼻咽頭ぬぐい液 |
| 結果までの判定時間 | 10~15分程度(その場でわかる) | 長い(その場ではわからない) | 30分程度(その場でわかる) |
| 精度 | キットによっては精度にばらつきがある | 比較的良い | PCRと比較して良くない |
| 免疫の有無※ | 過去にかかったかどうかが分かり、感染しにくい、人にうつしにくいかが分かる可能性。 | 現時点で感染しているかどうかしかわからない。 | 現時点で感染しているかどうかしかわからない。 |
| 検査従事者の感染の危険性 | 少ない | あり | あり |
※新型コロナウイルスの免疫の有無や免疫の持続性については、エビデンスが少なく、確定的なことは現時点では言及できません。
